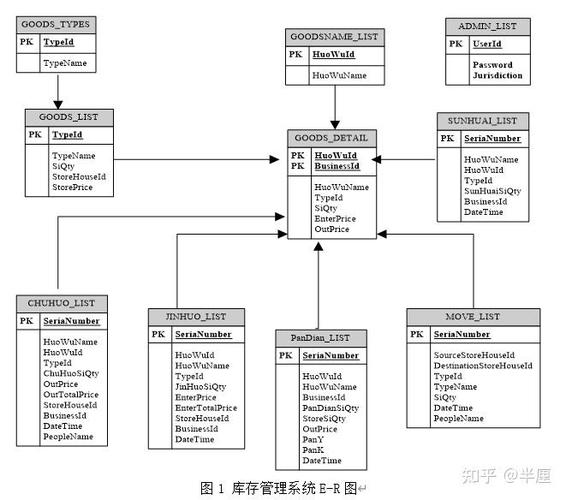
1. 中国药品注册数据库 : 该数据库涵盖了至目前为止所有在国内批准注册上市的药品,包括国产药品和进口药品的注册情况,支持模糊查询和组合查询,结果包括药品名称、规格、剂型、生产厂家、批准日期等信息。
2. 国家药品监督管理局数据查询: 该平台提供药品、医疗器械等相关数据的查询服务,用户可以通过邮件或联系相关部门解决数据问题。
3. 国家药品监管数据共享平台: 该平台提供数据查询、数据统计分析、数据可视化等服务,用户可以在这里找到详细的药品注册信息。
4. 国家药品监督管理局药品审评中心: 该中心发布了《中国上市药品目录集》,提供公开查询服务,用户可以通过该平台获取药品注册信息。
5. 国产药品查询: 该平台专门提供国产药品的查询服务,用户可以输入相关信息进行查询。
这些平台均由国家药品监督管理局提供,您可以根据具体需求选择合适的平台进行查询。如果您在使用过程中遇到任何问题,可以参考各平台的“常见问题”或联系相关部门获取帮助。
中国药品注册数据库:助力医药研发与监管透明化
随着医药行业的快速发展,药品注册数据库在保障药品安全、促进医药研发、提高监管透明度等方面发挥着越来越重要的作用。本文将详细介绍中国药品注册数据库的功能、查询方法以及其在医药行业中的应用。
一、中国药品注册数据库概述
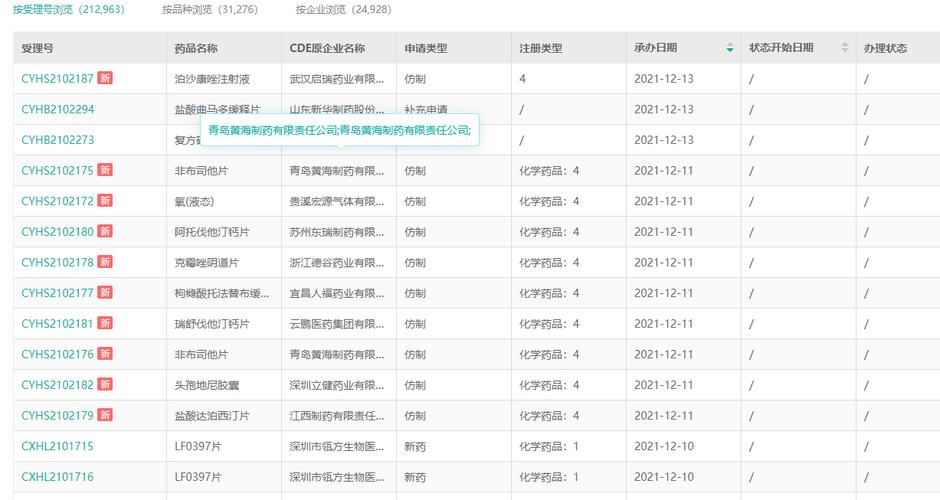
中国药品注册数据库是由国家药品监督管理局(NMPA)和药品审评中心(CDE)共同建设和维护的,旨在为医药研发人员、监管机构、医疗机构和公众提供药品注册信息的查询服务。
二、数据库功能
1. 药品注册信息查询:数据库收录了所有在中国境内注册的药品信息,包括药品名称、剂型、规格、生产厂家、批准文号、注册分类、受理号、审评结论等。
2. 审评审批进度查询:用户可以查询到药品注册申请的受理、审评、审批等各个阶段的进度信息。
3. 上市药品目录查询:数据库收录了在中国境内批准上市的药品信息,包括药品名称、剂型、规格、生产厂家、批准文号、上市日期等。
4. 药品不良反应监测:数据库收录了药品不良反应监测信息,包括不良反应报告、监测结果等。
三、查询方法
1. CDE官网查询:用户可以通过CDE官网的“信息公开”栏目,选择“受理品种信息”或“审评任务公示”进行查询。
2. 中国药品审评数据库查询:用户可以通过中国药品审评数据库进行查询,该数据库汇集了国家药监局、药品审评中心等官方资源,详尽收录了所有药品审评中心公布的受理号和办理状态。
3. 中国上市药品目录集数据库查询:用户可以通过《中国上市药品目录集》数据库进行查询,该数据库收录了在中国批准上市的创新药、改良型新药、化学药品新注册分类的仿制药以及通过质量和疗效一致性评价的药品的具体信息。
四、应用领域

1. 医药研发:药品注册数据库为医药研发人员提供了丰富的药品注册信息,有助于他们了解市场动态、评估研发风险、制定研发策略。
2. 监管机构:药品注册数据库为监管机构提供了药品注册信息的查询平台,有助于他们加强对药品注册的监管,提高监管效率。
3. 医疗机构:药品注册数据库为医疗机构提供了药品注册信息的查询平台,有助于他们了解药品的注册情况、合理用药、降低用药风险。
4. 公众:药品注册数据库为公众提供了药品注册信息的查询平台,有助于他们了解药品的注册情况、合理用药、保障用药安全。
中国药品注册数据库作为医药行业的重要信息资源,为医药研发、监管、医疗机构和公众提供了便捷的查询服务。随着数据库的不断更新和完善,其在医药行业中的应用将越来越广泛,为保障药品安全、促进医药行业发展发挥重要作用。